尿素
| 尿素 | |||
|---|---|---|---|
 | |||
| |||
 | |||
IUPAC名 Diaminomethanal 碳酰二胺 | |||
| 英文名 | Urea | ||
| 别名 | 脲 | ||
| 识别 | |||
CAS号 | 57-13-6 | ||
ChemSpider | 1143 | ||
SMILES |
| ||
InChI |
| ||
InChIKey | XSQUKJJJFZCRTK-UHFFFAOYAF | ||
Beilstein | 635724 | ||
Gmelin | 1378 | ||
DrugBank | DB03904 | ||
IUPHAR配体 | 4539 | ||
| 性质 | |||
化学式 | CH4N2O | ||
摩尔质量 | 60.06 g·mol−1 | ||
| 外观 | 无色無臭固體 | ||
密度 | 1.33 | ||
熔点 | 132.7 °C(分解) | ||
溶解性(水) | 108 g/100 mL (20 °C) 167 g/100 mL (40 °C) 251 g/100 mL (60 °C) 400 g/100 mL (80 °C) 733 g/100 mL (100 °C) | ||
pKb | 13.82 | ||
临界相对湿度 | 81% (20 °C) 73% (30 °C) | ||
| 结构 | |||
晶体结构 | 四方晶系 | ||
分子构型 | 平面三角 | ||
偶极矩 | 4.56 | ||
| 危险性 | |||
MSDS | ScienceLab.com | ||
| 主要危害 | 有毒 | ||
NFPA 704 |  1 2 0 | ||
| 相关物质 | |||
| 相关化学品 | 雙縮脲、硫脲 | ||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
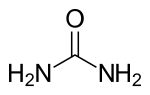
尿素是由碳、氮、氧和氢组成的有机化合物,又稱脲(與尿同音)。其化学公式为 CON2H4、(NH2)2CO 或 CN2H4O,分子质量60,国际非专利药品名称为 Carbamide(碳酰胺)。外观是无色晶体或粉末,是动物蛋白质代谢后的产物,通常用作植物的氮肥。
尿素在肝合成,是哺乳类动物排出的体内含氮代谢物。這代謝过程称为尿素循环。
尿素是第一种以人工合成无机物质而得到的有机化合物。活力论從此被推翻。
目录
1 发现
2 生理
3 生产
3.1 生产反应
4 应用
4.1 饲料添加剂
4.2 实验室应用
4.3 医学应用
4.4 纺织工业
5 脲
6 其他
7 外部链接
发现
1773年,伊莱尔·罗埃尔(Hilaire-Marin Rouelle)发现尿素。1828年,弗里德里希·维勒首次使用无机物质氰酸钾与硫酸铵人工合成了尿素。本来他打算合成氰酸铵(Ammonium cyanate,NH4NCO),卻得到了尿素。
由此证明了活力论是错误的,事实上开辟了有机化学。活力论认为无机物与有机物有根本性差異,所以无机物无法變成有机物。哺乳动物、两栖动物和一些鱼的尿中含有尿素;鸟和爬行动物排放的是尿酸,因為其氮代谢过程使用的水量比较少。
生理
尿素在肝脏产生后融入血液(人体内的浓度在每升2.5至7.5微摩尔/升之间),最后通过肾脏由尿排出。少量尿素由汗排出。
生物以二氧化碳、水、天冬氨酸和氨等化学物質合成尿素。促使尿素合成的代謝途徑是一種合成代谢,叫做尿素循环。此过程耗费能量,卻很必要。因为氨有毒,且是常见的新陈代谢产物,必须被消除。肝脏在合成尿素時,需要N-乙酰谷氨酸作為调节。
含氮废物具有毒性,产生自蛋白质和氨基酸的分解代谢过程。大多数生物必须再处理之。海生生物通常直接以氨的形式排入海水。陆地生物则转化氨为尿素或尿酸再排出。鸟和爬行动物通常排泄尿酸,其它动物(如哺乳动物)则是尿素。例外如,水生的蝌蚪排泄氨,但在其蜕变过程转为排泄尿素;大麥町狗主要排泄尿酸,不是尿素,因為其尿素循环中的一个转换酶的基因坏了。
哺乳动物以肝脏中的一个循环反应产生尿素。这循环最早在1932年被提出,其反应起点是氨的分解。1940年代澄清瓜氨酸和精氨基琥珀酸的作用后,它已完全被理解。在這循环中,来自氨和 L-天冬氨酸的氨基被转换为尿素,起中介作用的是 L-鳥氨酸、瓜氨酸、L-精氨酸-琥珀酸和 L-精氨酸。
尿素循环是哺乳动物和两栖动物排泄含氮代谢废物的主要途径。但別種生物亦然,如鸟類、无脊椎动物、昆虫、植物、酵母、真菌和微生物。
尿素對生物基本是废物,但仍有正面價值。比如,肾小管裡的尿素被引入肾皮质以提高其渗透浓度,促使水份从肾小管渗透回身體再利用。
生产
全世界每年工业的尿素产量约为十亿吨。中国目前尿素产能在6400万吨,年产量约5700万吨。商业尿素是通过氨与二氧化碳的反应生产的,成品尿素可以为药片状、颗粒状、片状、晶体或者溶液。尿素一般以药片或者颗粒的形式上市。
90%以上的生产的尿素被用作肥料。在所有的一般使用的估计氮肥料中尿素的含氮量最高(46.4%),因此相对而言其每氮营养的运输费最低。尿素在水中的可溶性非常高,因此非常适合被加在可溶的肥料中。
生产反应
商用尿素的原料是氨与二氧化碳。後者在以焦炭或烃(如天然气和石油)為原料生产氨的过程中,会大量产生。尿素因此直接从这些原料中就产生了。
尿素生产是一个平衡的化學反应,其反应物不完全成为反应结果。生产过程、設定的反应条件、如何处理未转化的反应物,皆可能不同。由於使用大量的反应物,未反应的反应物可用以生产其它产品,(如硝酸铵或硫酸铵),也可回收再投入反应。
实际的合成反应普遍认为应是在液相中分如下两大步完成的。
第一步是過量的液氨與乾冰反應為氨基甲酸铵。由於是可逆的放热反应,反應需要帶走熱能的設備。
- 2NH3 + CO2 ↔ H2N-COONH4 + 28千卡
第二步是加熱氨基甲酸铵為尿素;這步是一个可逆的吸热反应。反應需要帶走水分的設備。
- H2N-COONH4 ↔ (NH2)2CO + H2O - 3.6千卡
尿素的反应总式为:
- 2NH3+CO2 → CO(NH2)2+H2O
表達在该公式的生产反应總體上为一个可逆的放热反应。
尿素在生产中通常伴随着副产品,如甲醇,也可用来制造下游产品,如三聚氰胺等。
应用

1965年中國上海市吴泾化工厂尿素厂
尿素在商业上,可作為:
- 特殊塑料的原料,尤其是尿素甲醛樹脂
- 某些胶類的原料
肥料和饲料的成分- 取代防冻的盐撒在街道,优点是不使金属腐蚀
- 加强香烟的氣味
- 賦予工业生产的椒鹽卷餅棕色
- 某些洗发剂、清洁剂的成分
- 急救用制冷包的成分,因為尿素与水的反應會吸热
- 处理柴油机、发动机、热力发电厂的废气,尤其可降低其中氮氧化物的含量
- 催雨剂的成分〈配合盐〉
- 过去用来分离石蜡,因為尿素能形成包合物
- 耐火材料
- 環保引擎燃料的成分
美白牙齿产品的成分- 為化學肥料
饲料添加剂
人类粮食资源與蛋白质的短缺,也造成饲料工业一大难题。業者積極尋找蛋白质的新來源,並擴及蛋白質以外的氮來源,例如含氮量高的尿素。
1897年,Waesk 等人提出反刍动物能转化非蛋白質氮为菌体蛋白質的想法。1949年,C. J. Watson 等人餵食绵羊含有N15标记的尿素胶囊,4天后在绵羊血液、肝脏、肾脏中檢驗出含有N15的蛋白质。這证实了反刍动物可以利用非蛋白質氮。同年 J. K. Looli 等人以尿素當作唯一氮源餵食绵羊,发现绵羊能夠正氮平衡,表明绵羊瘤胃裡的微生物能利用尿素合成其生长所需的10种必需氨基酸。自此,尿素及尿素化合物成為反刍动物的饲料添加剂了。
实验室应用
尿素能非常有效的使蛋白质变性,尤其能非常有效地破坏非共价键结合的蛋白质。这特点可以提高某些蛋白质的可溶性,其浓度可达10摩尔体积。尿素也可用来制造硝酸尿素。
医学应用
皮肤科以含有尿素的某些药剂来提高皮肤的湿度。非手术摘除的指甲使用的封闭敷料中,含有40%的尿素。
测试幽門螺桿菌存在的碳-14-呼气试验,使用了含有碳14或碳13标记的尿素。因為幽門螺桿菌的尿素酶使用尿素来製造氨,以提高其周边胃里的pH值。同样原理也可测试生活在动物胃中的类似细菌。
纺织工业
尿素是纺织工业在染色和印刷時的重要辅助剂,能提高颜料可溶性,並使纺织品染色后保持一定的湿度。
脲
脲是化合物,含有官能团RR'N-CO-NRR'。这官能团的羰基帶著两个有机的氨基。实验室中,光气可与此二氨基反应。脲類化合物包括过氧化脲、尿囊素、乙内酰脲。脲与缩二脲非常接近。脲的化學结构与酰胺、氨基甲酸、双偶氮化合物、碳二亚胺等接近。
其他
- 硫脲
- 硫酰胺
外部链接
- 中国尿素网
- 中国种植业大观·肥料卷·尿素
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||
|